Đánh giá kết quả điều trị tân bổ trợ ung thư vú tại bệnh viện ung bướu Đà Nẵng
Đặt vấn đề: Hóa trị tân bổ trợ ung thư vú giúp giảm giai đoạn bướu tại chỗ, giảm độ rộng phẫu thuật.
Cải thiện sống còn khi đạt được đáp ứng bệnh học hoàn toàn (pCR).
Đối tượng và phương pháp nghiên cứu: Nghiên cứu hồi cứu mô tả, cắt ngang. Tiêu chuẩn chọn
bệnh: BN UTV giai đoạn T2-4,N0-3,M0 được hóa trị tân bổ trợ. Loại trừ các trường hợp ung thư vú tại chỗ
hoặc đã điều trị trước đó.
Kết quả: Độ tuổi trung bình là 48, kích thước bướu trung bình 6.0 cm, Đa số là carcinoma ống tuyến vú
dạng NOS (97,8%) và grad 2 (85,6%). Nội tiết dương tính trong 57%, HER-2 dương tính trong 38,7% và có
18,3% nhóm tam âm. Phác đồ kết hợp anthacycline và Taxane chiếm 94,7%, phác đồ có Trastuzumab chiếm
25% trong nhóm Her2 (+). Có 8,3% bệnh tiến triển trong khi hóa trị. Về phẫu thuật: Phẫu thuật bảo tồn chiếm
(20,5%), Tạo hình vú tức thì chiếm 6,8%, Đoạn nhũ toàn bộ chiếm 71,6%. Có 4,3% được phẫu thuật sinh thiết
hạch gác. Tình trạng Her2 khác biệt có ý nghĩa thống kê giữa 2 nhóm đạt và không đạt pCR. Nhóm nội tiết âm
tính, Ki67 cao và nhóm tam âm có tỷ lệ đạt pCR cao hơn nhưng không có ý nghĩa thống kê.
Kết luận: Hóa trị tân bổ trợ giúp giảm giai đoạn tại chỗ, tăng tỷ lệ phẫu thuật bảo tồn và tạo hình vú.
Tình trạng Her2 có mối tương quan với tỷ lệ đạt đáp ứng bệnh học hoàn toàn (pCR).

Trang 1

Trang 2
Trang 3
Trang 4
Trang 5

Trang 6
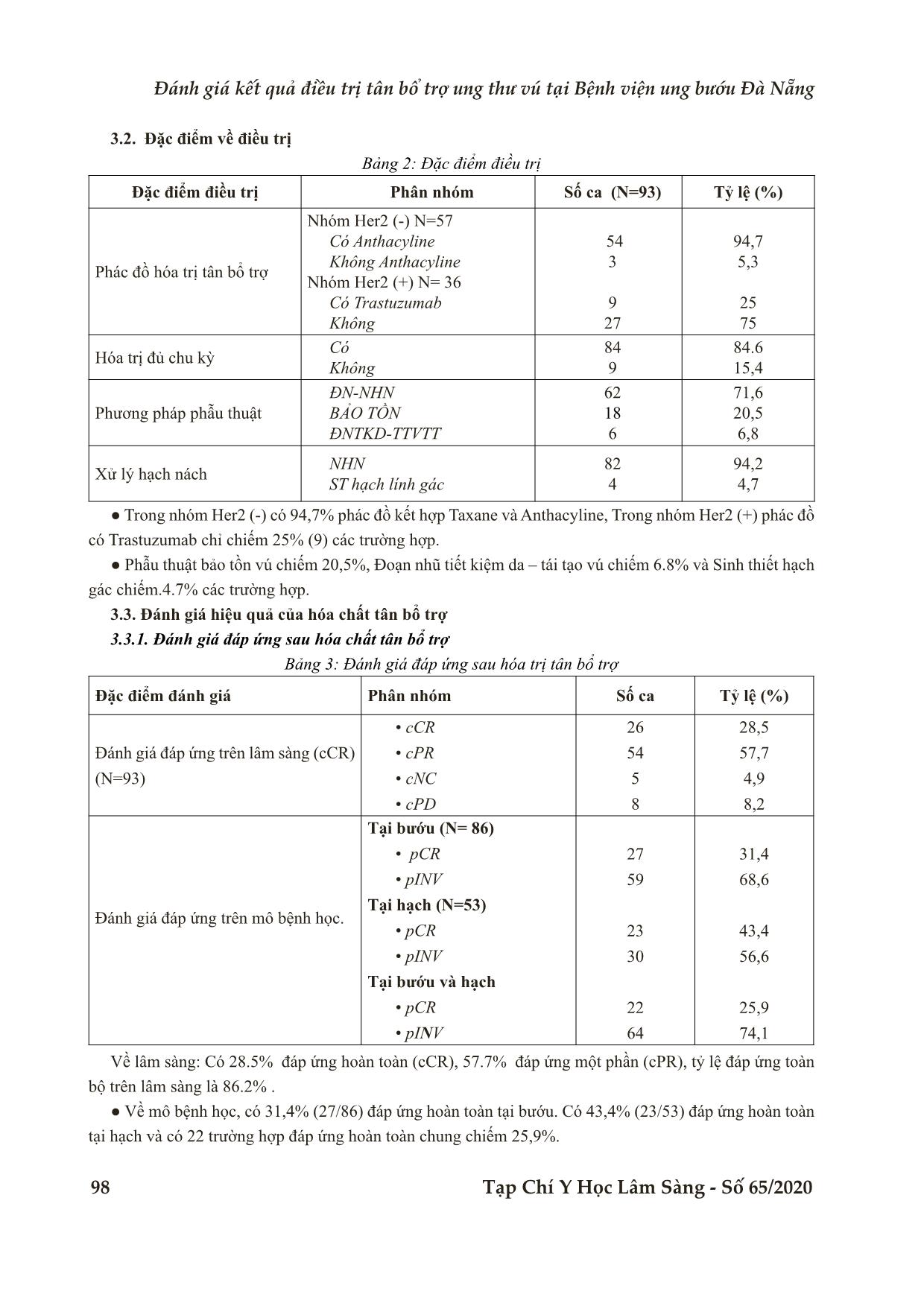
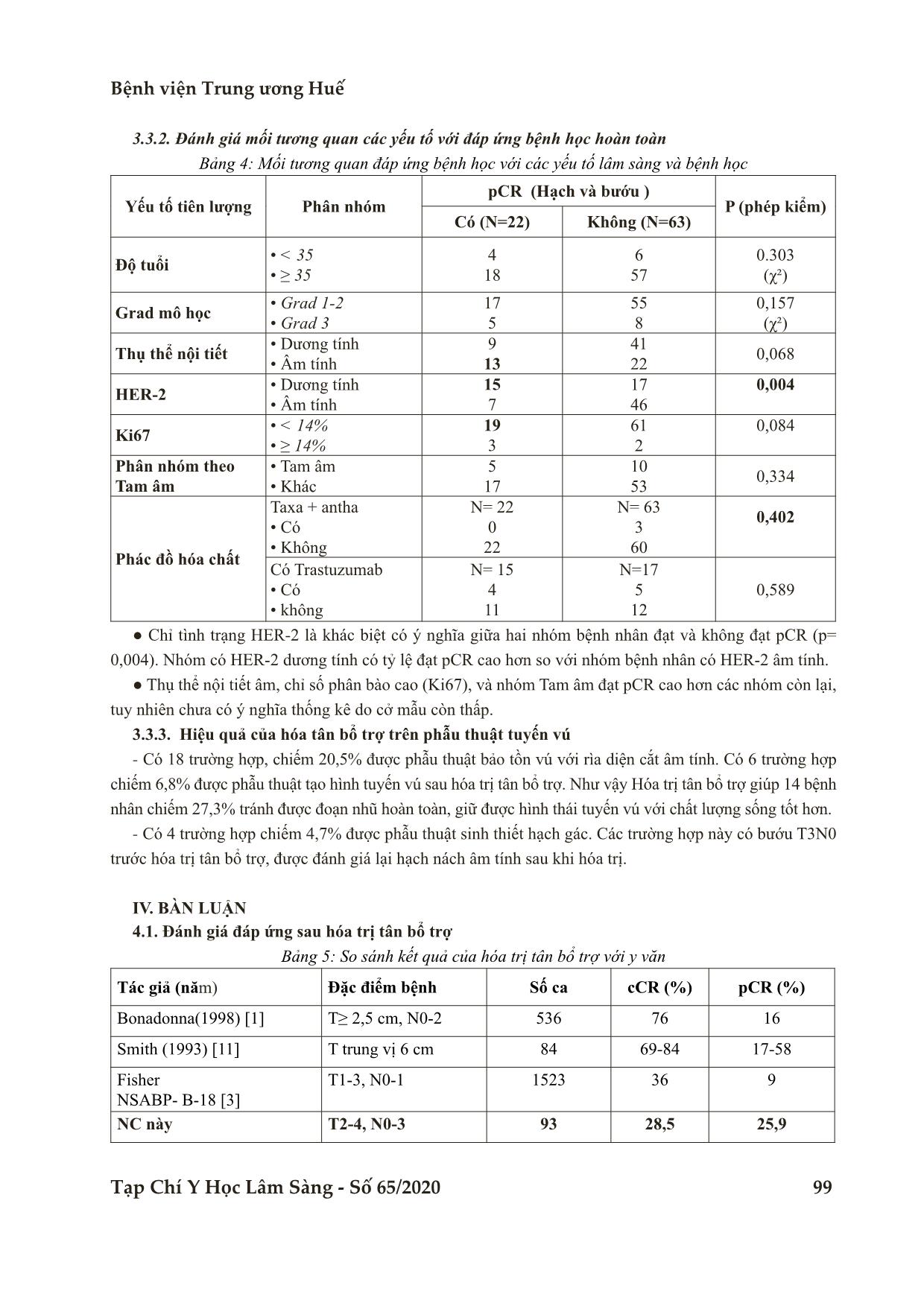
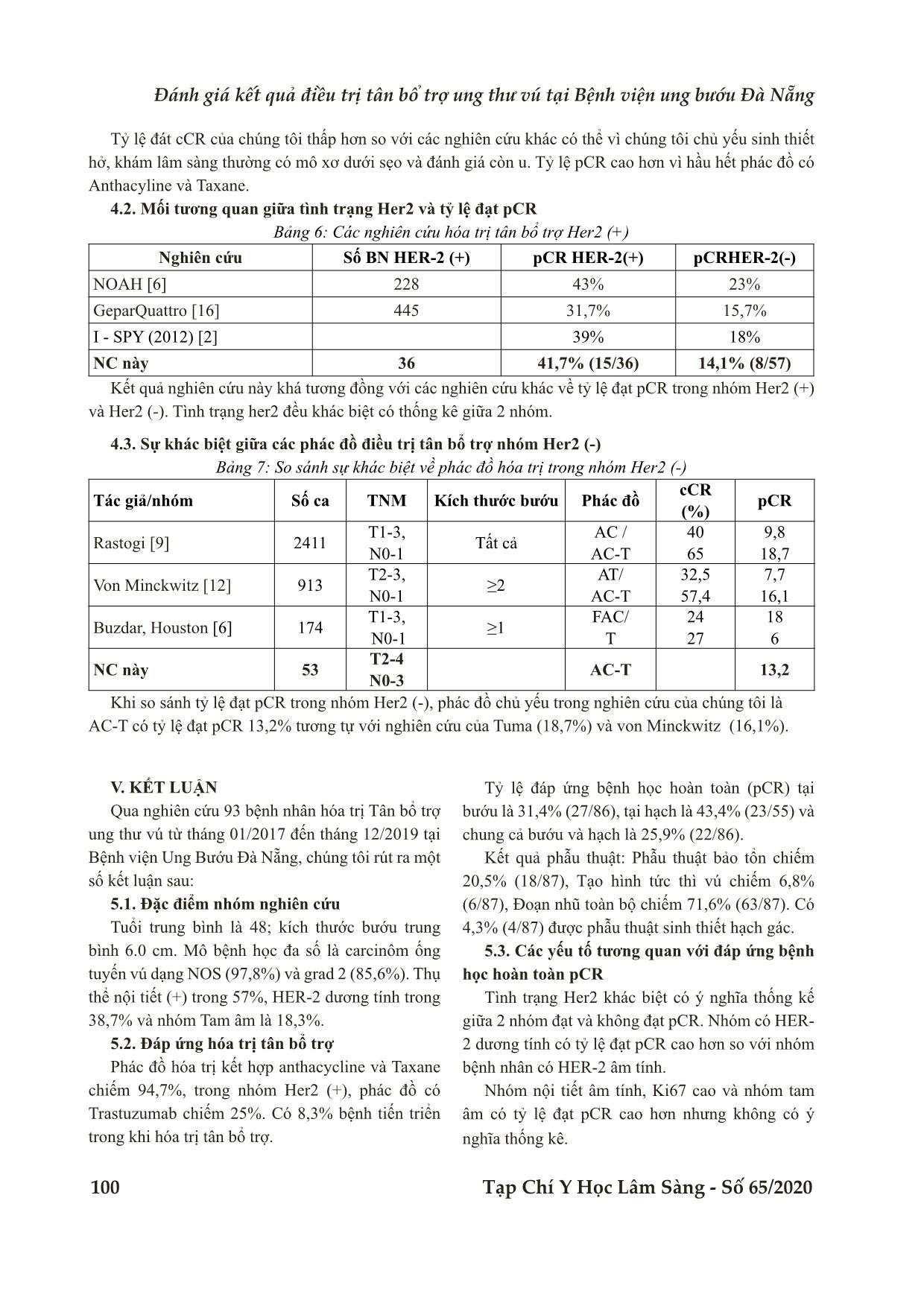
Tóm tắt nội dung tài liệu: Đánh giá kết quả điều trị tân bổ trợ ung thư vú tại bệnh viện ung bướu Đà Nẵng

Bệnh viện Trung ương Huế 96 Tạp Chí Y Học Lâm Sàng - Số 65/2020 Nghiên cứu ĐÁNH GIÁ KẾT QUẢ ĐIỀU TRỊ TÂN BỔ TRỢ UNG THƯ VÚ TẠI BỆNH VIỆN UNG BƯỚU ĐÀ NẴNG Bùi Thanh Tình1*, Phạm Thanh Hải1, Lê Trung Quân1, Nguyễn Xuân Quang1 DOI: 10.38103/jcmhch.2020.65.14 TÓM TẮT Đặt vấn đề: Hóa trị tân bổ trợ ung thư vú giúp giảm giai đoạn bướu tại chỗ, giảm độ rộng phẫu thuật. Cải thiện sống còn khi đạt được đáp ứng bệnh học hoàn toàn (pCR). Đối tượng và phương pháp nghiên cứu: Nghiên cứu hồi cứu mô tả, cắt ngang. Tiêu chuẩn chọn bệnh: BN UTV giai đoạn T2-4,N0-3,M0 được hóa trị tân bổ trợ. Loại trừ các trường hợp ung thư vú tại chỗ hoặc đã điều trị trước đó. Kết quả: Độ tuổi trung bình là 48, kích thước bướu trung bình 6.0 cm, Đa số là carcinoma ống tuyến vú dạng NOS (97,8%) và grad 2 (85,6%). Nội tiết dương tính trong 57%, HER-2 dương tính trong 38,7% và có 18,3% nhóm tam âm. Phác đồ kết hợp anthacycline và Taxane chiếm 94,7%, phác đồ có Trastuzumab chiếm 25% trong nhóm Her2 (+). Có 8,3% bệnh tiến triển trong khi hóa trị. Về phẫu thuật: Phẫu thuật bảo tồn chiếm (20,5%), Tạo hình vú tức thì chiếm 6,8%, Đoạn nhũ toàn bộ chiếm 71,6%. Có 4,3% được phẫu thuật sinh thiết hạch gác. Tình trạng Her2 khác biệt có ý nghĩa thống kê giữa 2 nhóm đạt và không đạt pCR. Nhóm nội tiết âm tính, Ki67 cao và nhóm tam âm có tỷ lệ đạt pCR cao hơn nhưng không có ý nghĩa thống kê. Kết luận: Hóa trị tân bổ trợ giúp giảm giai đoạn tại chỗ, tăng tỷ lệ phẫu thuật bảo tồn và tạo hình vú. Tình trạng Her2 có mối tương quan với tỷ lệ đạt đáp ứng bệnh học hoàn toàn (pCR). Từ khóa: Hóa trị tân bổ trợ, Ung thư vú, Đáp ứng bệnh học toàn toàn (pCR), ABSTRACT EVALUATION OF THE RESULTS OF NEOADJUVANT CHEMOTHERAPY FOR BREAST CANCER AT DA NANG ONCOLOGY HOSPITAL Bui Thanh Tinh1*, Pham Thanh Hai1, Le Trung Quan1, Nguyen Xuan Quang1 Background: Neoadjuvant chemotherapy for breast cancer was used to downstaging tumours to facili- tate breast-conserving surgery. Methods: A descriptive retrospective study of 93 breast cancer patients at Da Nang Oncology Hospital from January 2017 to December 2019. Patients diagnosed with locally advanced breast cancer cT2-4N0- 3M0. Exclude cases of Ductal carcinoma in situ from breast or previously treated. Results: an average age of 48, an average tumor size of 6.0 cm, the majority were Invasive ductal carci- noma (97.8%) and grade 2 ( 85.6%). Hormon receptor positive in 57%, HER-2 positive in 38.7% and 18.3% triple negative Breast cancer. The combination chemotherapy regimen Anthacycline and Taxane accounted 1 Khoa ngoại 3, Bệnh viện Ung Bướu Đà Nẵng, Đà Nẵng. - Ngày nhận bài (Received): 1/10/2020; Ngày phản biện (Revised): 06/10/ 2020; - Ngày đăng bài (Accepted): 04 /12 /2020 - Người phản hồi (Corresponding author): Bùi Thanh Tình - Email: dr.thanhtinh.ubdn@gmail.com; ĐT: 0983.885.350 Đánh giá kết quả điều trị tân bổ trợ ung thư vú tại Bệnh viện u g bướu Đà Nẵng Bệnh viện Trung ương Huế Tạp Chí Y Học Lâm Sàng - Số 65/2020 97 I. ĐẶT VẤN ĐỀ Điều trị tân bổ trợ hay điều trị trước phẫu thuật đã được sử dụng trong 2 thập kỷ qua để giảm giai đoạn ung thư vú tiến triển tại chỗ, chuyển từ không mổ được thành mổ được và có thể bảo tồn thay vì đoạn nhũ [8], [10]. Một số nghiên cứu, bao gồm nghiên cứu NSABP 18 đã chứng minh điều trị cùng phác đồ trước và sau phẫu thuật có kết quả tương tự và đáp ứng bệnh học hoàn toàn (pCR) có mối tương quan với cải thiện DFS và OS [3], [7], [9]. Chọn lựa phác đồ điều trị tương tự như hóa trị bổ trợ, hóa trị tân bổ trợ đạt đáp ứng lâm sàng 60- 90%, đáp ứng trên giải phẫu bệnh khoảng 10-30% [4], [5]. Tại bệnh viện Ung bướu Đà nẵng chưa có công trình nghiên cứu nào về đề tài này vì vậy Chúng tôi tiến hành nghiên cứu với các mục tiêu sau: MỤC TIÊU NGHIÊN CỨU 1. Đánh giá kết quả điều trị Tân bổ trợ 2. Đánh giá các yếu tố tương quan với đáp ứng bệnh học hoàn toàn pCR II. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU 2.1. Đối tượng nghiên cứu Tiêu chí chọn mẫu ● Bệnh nhân được chẩn đoán UTV giai đoạn T2- 4N0-3M0 được điều trị hóa trị tân bổ trợ tại BVUB Đà Nẵng từ 01/2017 đến 12/2019. Có đầy đủ thông tin hồ sơ. Tiêu chí loại trừ ● Carcinôm tuyến tại chỗ. ● Bệnh đã được chẩn đoán và điều trị trước đó. 2.2. Phương pháp nghiên cứu Thiết kế nghiên cứu Nghiên cứu Hồi cứu mô tả cắt ngang, không so sánh. 2.3. Xử lý số liệu ● Tính toán bằng phần mềm spss 20.0, kết quả được trình bày dạng bảng, biểu đồ, hình ảnh và mô tả. ● Thống kê phân tích so sánh hiệu quả điều trị ở các phân nhóm sinh học về tỉ lệ đáp ứng và phép kiểm chi bình phương và T-test, khoảng tin cậy 95% được xác định kèm theo, p<0,05 được xem là có ý nghĩa thống kê. III. KẾT QUẢ 3.1. Đặc Điểm Lâm Sàng và cận lâm sàng Bảng 1: Đặc điểm lâm sàng và mô bệnh học Đặc điểm Phân nhóm Số ca (N=93) Tỷ lệ % Độ tuổi • < 35 tuổi • ≥ 35 tuổi 11 82 15.4 84.6 Xếp hạng T • cT2 • cT3 • cT4 23 35 35 24,7 37,6 37,6 Xếp hạng N • cNo • cN1 • cN2 • cN3 28 30 21 14 30,1 32,3 22,6 15,1 Đặt clip đánh dấu • Có • Không 26 67 28,1 71,9 Loại GPB • Ống tuyến vú • Tiểu thùy 91 2 97,8 2,2 Grade mô học • Grad 1 • Grad 2 • Grad 3 0 80 13 0 85,6 14,4 HER-2/neu • Âm tính • Dương tính 57 36 61,3 38,7 Thụ thể ER, PR • Âm tính • Dương tính 40 53 43 57 Tuổi > 35% chiếm 84,6%, Bướu T2 24,7%. Hạch cN3 chiếm 15,1%, Nội tiết dương tính trong 57%. HER-2 dương tính trong 38.7%. for 94.7%, Trastuzumab-based regimen accounted for 25%. There was 8.3% progression of disease during neoadjuvant chemotherapy. About Surgery: Breast- conserving surgery in 20.5%, Breast reconstruction in 6.8%, Mastectomy in 71.6%, Sentinel lymph node biopsy in 4.3%. Her2 status was significantly different between the groups with and without pCR.. Endocrine receptors are negative, Ki67 is high, and Triple nega- tive has a higher rate of pCR but not statistically significant. Conclusion: Neoadjuvant chemotherapy helps to downstaging tumours to facilitate breast-conserving surgery. Her2 status is correlated with the rate of complete pathological response (pCR). Keyword: Neoadjuvant chemotherapy, Breast cancer, Pathologic complete response. Bệnh viện Trung ương Huế 98 Tạp Chí Y Học Lâm Sàng - Số 65/2020 3.2. Đặc điểm về điều trị Bảng 2: Đặc điểm điều trị Đặc điểm điều trị Phân nhóm Số ca (N=93) Tỷ lệ (%) Phác đồ hóa trị tân bổ trợ Nhóm Her2 (-) N=57 Có Anthacyline Không Anthacyline Nhóm Her2 (+) N= 36 Có Trastuzumab Không 54 3 9 27 94,7 5,3 25 75 Hóa trị đủ chu kỳ Có Không 84 9 84.6 15,4 Phương pháp phẫu thuật ĐN-NHN BẢO TỒN ĐNTKD-TTVTT 62 18 6 71,6 20,5 6,8 Xử lý hạch nách NHN ST hạch lính gác 82 4 94,2 4,7 ● Trong nhóm Her2 (-) có 94,7% phác đồ kết hợp Taxane và Anthacyline, Trong nhóm Her2 (+) phác đồ có Trastuzumab chỉ chiếm 25% (9) các trường hợp. ● Phẫu thuật bảo tồn vú chiếm 20,5%, Đoạn nhũ tiết kiệm da – tái tạo vú chiếm 6.8% và Sinh thiết hạch gác chiếm.4.7% các trường hợp. 3.3. Đánh giá hiệu quả của hóa chất tân bổ trợ 3.3.1. Đánh giá đáp ứng sau hóa chất tân bổ trợ Bảng 3: Đánh giá đáp ứng sau hóa trị tân bổ trợ Đặc điểm đánh giá Phân nhóm Số ca Tỷ lệ (%) Đánh giá đáp ứng trên lâm sàng (cCR) (N=93) • cCR • cPR • cNC • cPD 26 54 5 8 28,5 57,7 4,9 8,2 Đánh giá đáp ứng trên mô bệnh học. Tại bướu (N= 86) • pCR • pINV Tại hạch (N=53) • pCR • pINV Tại bướu và hạch • pCR • pINV 27 59 23 30 22 64 31,4 68,6 43,4 56,6 25,9 74,1 Về lâm sàng: Có 28.5% đáp ứng hoàn toàn (cCR), 57.7% đáp ứng một phần (cPR), tỷ lệ đáp ứng toàn bộ trên lâm sàng là 86.2% . ● Về mô bệnh học, có 31,4% (27/86) đáp ứng hoàn toàn tại bướu. Có 43,4% (23/53) đáp ứng hoàn toàn tại hạch và có 22 trường hợp đáp ứng hoàn toàn chung chiếm 25,9%. Đánh giá kết quả điều trị tân bổ trợ ung thư vú tại Bệnh viện u g bướu Đà Nẵng Bệnh viện Trung ương Huế Tạp Chí Y Học Lâm Sàng - Số 65/2020 99 3.3.2. Đánh giá mối tương quan các yếu tố với đáp ứng bệnh học hoàn toàn Bảng 4: Mối tương quan đáp ứng bệnh học với các yếu tố lâm sàng và bệnh học Yếu tố tiên lượng Phân nhóm pCR (Hạch và bướu ) P (phép kiểm) Có (N=22) Không (N=63) Độ tuổi • < 35 • ≥ 35 4 18 6 57 0.303 (χ²) Grad mô học • Grad 1-2 • Grad 3 17 5 55 8 0,157 (χ²) Thụ thể nội tiết • Dương tính • Âm tính 9 13 41 22 0,068 HER-2 • Dương tính • Âm tính 15 7 17 46 0,004 Ki67 • < 14% • ≥ 14% 19 3 61 2 0,084 Phân nhóm theo Tam âm • Tam âm • Khác 5 17 10 53 0,334 Phác đồ hóa chất Taxa + antha • Có • Không N= 22 0 22 N= 63 3 60 0,402 Có Trastuzumab • Có • không N= 15 4 11 N=17 5 12 0,589 ● Chỉ tình trạng HER-2 là khác biệt có ý nghĩa giữa hai nhóm bệnh nhân đạt và không đạt pCR (p= 0,004). Nhóm có HER-2 dương tính có tỷ lệ đạt pCR cao hơn so với nhóm bệnh nhân có HER-2 âm tính. ● Thụ thể nội tiết âm, chỉ số phân bào cao (Ki67), và nhóm Tam âm đạt pCR cao hơn các nhóm còn lại, tuy nhiên chưa có ý nghĩa thống kê do cở mẫu còn thấp. 3.3.3. Hiệu quả của hóa tân bổ trợ trên phẫu thuật tuyến vú - Có 18 trường hợp, chiếm 20,5% được phẫu thuật bảo tồn vú với rìa diện cắt âm tính. Có 6 trường hợp chiếm 6,8% được phẫu thuật tạo hình tuyến vú sau hóa trị tân bổ trợ. Như vậy Hóa trị tân bổ trợ giúp 14 bệnh nhân chiếm 27,3% tránh được đoạn nhũ hoàn toàn, giữ được hình thái tuyến vú với chất lượng sống tốt hơn. - Có 4 trường hợp chiếm 4,7% được phẫu thuật sinh thiết hạch gác. Các trường hợp này có bướu T3N0 trước hóa trị tân bổ trợ, được đánh giá lại hạch nách âm tính sau khi hóa trị. IV. BÀN LUẬN 4.1. Đánh giá đáp ứng sau hóa trị tân bổ trợ Bảng 5: So sánh kết quả của hóa trị tân bổ trợ với y văn Tác giả (năm) Đặc điểm bệnh Số ca cCR (%) pCR (%) Bonadonna(1998) [1] T≥ 2,5 cm, N0-2 536 76 16 Smith (1993) [11] T trung vị 6 cm 84 69-84 17-58 Fisher NSABP- B-18 [3] T1-3, N0-1 1523 36 9 NC này T2-4, N0-3 93 28,5 25,9 Bệnh viện Trung ương Huế 100 Tạp Chí Y Học Lâm Sàng - Số 65/2020 Tỷ lệ đát cCR của chúng tôi thấp hơn so với các nghiên cứu khác có thể vì chúng tôi chủ yếu sinh thiết hở, khám lâm sàng thường có mô xơ dưới sẹo và đánh giá còn u. Tỷ lệ pCR cao hơn vì hầu hết phác đồ có Anthacyline và Taxane. 4.2. Mối tương quan giữa tình trạng Her2 và tỷ lệ đạt pCR Bảng 6: Các nghiên cứu hóa trị tân bổ trợ Her2 (+) Nghiên cứu Số BN HER-2 (+) pCR HER-2(+) pCRHER-2(-) NOAH [6] 228 43% 23% GeparQuattro [16] 445 31,7% 15,7% I - SPY (2012) [2] 39% 18% NC này 36 41,7% (15/36) 14,1% (8/57) Kết quả nghiên cứu này khá tương đồng với các nghiên cứu khác về tỷ lệ đạt pCR trong nhóm Her2 (+) và Her2 (-). Tình trạng her2 đều khác biệt có thống kê giữa 2 nhóm. 4.3. Sự khác biệt giữa các phác đồ điều trị tân bổ trợ nhóm Her2 (-) Bảng 7: So sánh sự khác biệt về phác đồ hóa trị trong nhóm Her2 (-) Tác giả/nhóm Số ca TNM Kích thước bướu Phác đồ cCR(%) pCR Rastogi [9] 2411 T1-3, N0-1 Tất cả AC / AC-T 40 65 9,8 18,7 Von Minckwitz [12] 913 T2-3, N0-1 ≥2 AT/ AC-T 32,5 57,4 7,7 16,1 Buzdar, Houston [6] 174 T1-3, N0-1 ≥1 FAC/ T 24 27 18 6 NC này 53 T2-4N0-3 AC-T 13,2 Khi so sánh tỷ lệ đạt pCR trong nhóm Her2 (-), phác đồ chủ yếu trong nghiên cứu của chúng tôi là AC-T có tỷ lệ đạt pCR 13,2% tương tự với nghiên cứu của Tuma (18,7%) và von Minckwitz (16,1%). V. KẾT LUẬN Qua nghiên cứu 93 bệnh nhân hóa trị Tân bổ trợ ung thư vú từ tháng 01/2017 đến tháng 12/2019 tại Bệnh viện Ung Bướu Đà Nẵng, chúng tôi rút ra một số kết luận sau: 5.1. Đặc điểm nhóm nghiên cứu Tuổi trung bình là 48; kích thước bướu trung bình 6.0 cm. Mô bệnh học đa số là carcinôm ống tuyến vú dạng NOS (97,8%) và grad 2 (85,6%). Thụ thể nội tiết (+) trong 57%, HER-2 dương tính trong 38,7% và nhóm Tam âm là 18,3%. 5.2. Đáp ứng hóa trị tân bổ trợ Phác đồ hóa trị kết hợp anthacycline và Taxane chiếm 94,7%, trong nhóm Her2 (+), phác đồ có Trastuzumab chiếm 25%. Có 8,3% bệnh tiến triển trong khi hóa trị tân bổ trợ. Tỷ lệ đáp ứng bệnh học hoàn toàn (pCR) tại bướu là 31,4% (27/86), tại hạch là 43,4% (23/55) và chung cả bướu và hạch là 25,9% (22/86). Kết quả phẫu thuật: Phẫu thuật bảo tổn chiếm 20,5% (18/87), Tạo hình tức thì vú chiếm 6,8% (6/87), Đoạn nhũ toàn bộ chiếm 71,6% (63/87). Có 4,3% (4/87) được phẫu thuật sinh thiết hạch gác. 5.3. Các yếu tố tương quan với đáp ứng bệnh học hoàn toàn pCR Tình trạng Her2 khác biệt có ý nghĩa thống kế giữa 2 nhóm đạt và không đạt pCR. Nhóm có HER- 2 dương tính có tỷ lệ đạt pCR cao hơn so với nhóm bệnh nhân có HER-2 âm tính. Nhóm nội tiết âm tính, Ki67 cao và nhóm tam âm có tỷ lệ đạt pCR cao hơn nhưng không có ý nghĩa thống kê. Đánh giá kết quả điều trị tân bổ trợ ung thư vú tại Bệnh viện ung bướu Đà Nẵng Bệnh viện Trung ương Huế Tạp Chí Y Học Lâm Sàng - Số 65/2020 101 1. Bonadonna G. et al. (1995), “Primary chemotherapy in surgically resectable breast cancer”, CA Cancer J Clin. 45 (4), pp. 227-243.. 2. Esserman L. J. et al. (2012), “Pathologic complete response predicts recurrence-free survival more effectively by cancer subset: results from the I-SPY 1 TRIAL--CALGB 150007/150012, ACRIN 6657”, J Clin Oncol. 30 (26), pp. 3242-3249. 3. Fisher B. et al. (1997), “Effect of preoperative chemotherapy on local-regional disease in women with operable breast cancer: findings from National Surgical Adjuvant Breast and Bowel Project B-18”, J Clin Oncol. 15 (7), pp. 2483-2493.. 4. Kaufmann M. et al. (2006), “Recommendations from an international expert panel on the use of neoadjuvant (primary) systemic treatment of operable breast cancer: an update”, J Clin Oncol. 24 (12), pp. 1940-1949.. 5. Kaufmann M. et al. (2012), “Recommendations from an international consensus conference on the current status and future of neoadjuvant systemic therapy in primary breast cancer”, Ann Surg Oncol. 19 (5), pp. 1508-1516.. 6. Mathew J. et al. (2009), “Primary endocrine therapy in locally advanced breast cancers--the Nottingham experience”, Breast Cancer Res Treat. 113 (2), pp. 403-407.. 7. Mauri D. et al. (2005), “Neoadjuvant versus adjuvant systemic treatment in breast cancer: a meta-analysis”, J Natl Cancer Inst. 97 (3), pp. 188-194.. 8. Perloff M. et al. (1982), “Chemotherapy before and after mastectomy in stage III breast cancer”, Arch Surg. 117 (7), pp. 879-881.. 9. Rastogi P. et al. (2008), “Preoperative chemotherapy: updates of National Surgical Adjuvant Breast and Bowel Project Protocols B-18 and B-27”, J Clin Oncol. 26 (5), pp. 778-785.. 10. Schick P. et al. (1983), “Preoperative chemotherapy followed by mastectomy for locally advanced breast cancer”, J Surg Oncol. 22 (4), pp. 278-282.. 11. Smith I. C. et al. (2002), “Neoadjuvant chemotherapy in breast cancer: significantly enhanced response with docetaxel”, J Clin Oncol. 20 (6), pp. 1456-1466.. 12. von Minckwitz G. et al. (2012), “Definition and impact of pathologic complete response on prognosis after neoadjuvant chemotherapy in various intrinsic breast cancer subtypes”, J Clin Oncol. 30 (15), pp. 1796-1804.. TÀI LIỆU THAM KHẢO
File đính kèm:
 danh_gia_ket_qua_dieu_tri_tan_bo_tro_ung_thu_vu_tai_benh_vie.pdf
danh_gia_ket_qua_dieu_tri_tan_bo_tro_ung_thu_vu_tai_benh_vie.pdf

