Điều chế thanh nano gadolini hydroxit và khảo sát hoạt tính xúc tác của hệ UV/H ₂O ₂/Gd(OH)₃
Trong những năm gần đây, quá trình oxy
hóa khử nâng cao đã được chứng minh là một
trong những phương pháp hiệu quả, kinh tế cao và
có khả năng xử lý nguồn nước ô nhiễm hợp chất
hữu cơ tốt [1, 2]. Bản chất của quá trình oxy hóa
khử nâng cao là tạo ra gốc tự do .OH, một sản phẩm
trung gian, có hoạt tính oxy hóa rất cao (E0 = 2,8 V),
chỉ sau flo (E0 = 3,05 V) [1]. Gốc tự do hydoxy được
tạo ra bởi các tác nhân H2O2, O3, H2O, v.v. dưới tác
dụng của tia UV hoặc UV/xúc tác rắn [1-3]. Vật liệu
xúc tác rắn thông thường được sử dụng là các hợp
chất của kim loại chuyển tiếp như oxit, hydroxit,
sunfua, v.v. Trong đó, quá trình phản ứng oxy hóa
khử nâng cao trên chất xúc tác dị thể vẫn chưa
được nghiên cứu đầy đủ. Số lượng công trình được
công bố về hệ xúc tác UV/H2O2/xúc tác rắn vẫn còn
rất khiêm tốn, tiêu biểu là hệ UV/H2O2/ZnO xúc
tác quá trình xử lý nước thải của ngành công
nghiệp sữa [4], hoặc UV/H2O2/TiO2 và
UV/H2O2/TiO2+Zeolit được các tác giả nghiên cứu
xúc tác cho quá trình phân hủy các chất màu trong
nước thải rỉ đường và nước thải chứa chất màu azo
trong sản phẩm thương mại [5, 6].

Trang 1

Trang 2
Trang 3
Trang 4
Trang 5
Trang 6
Trang 7

Trang 8
Tóm tắt nội dung tài liệu: Điều chế thanh nano gadolini hydroxit và khảo sát hoạt tính xúc tác của hệ UV/H ₂O ₂/Gd(OH)₃

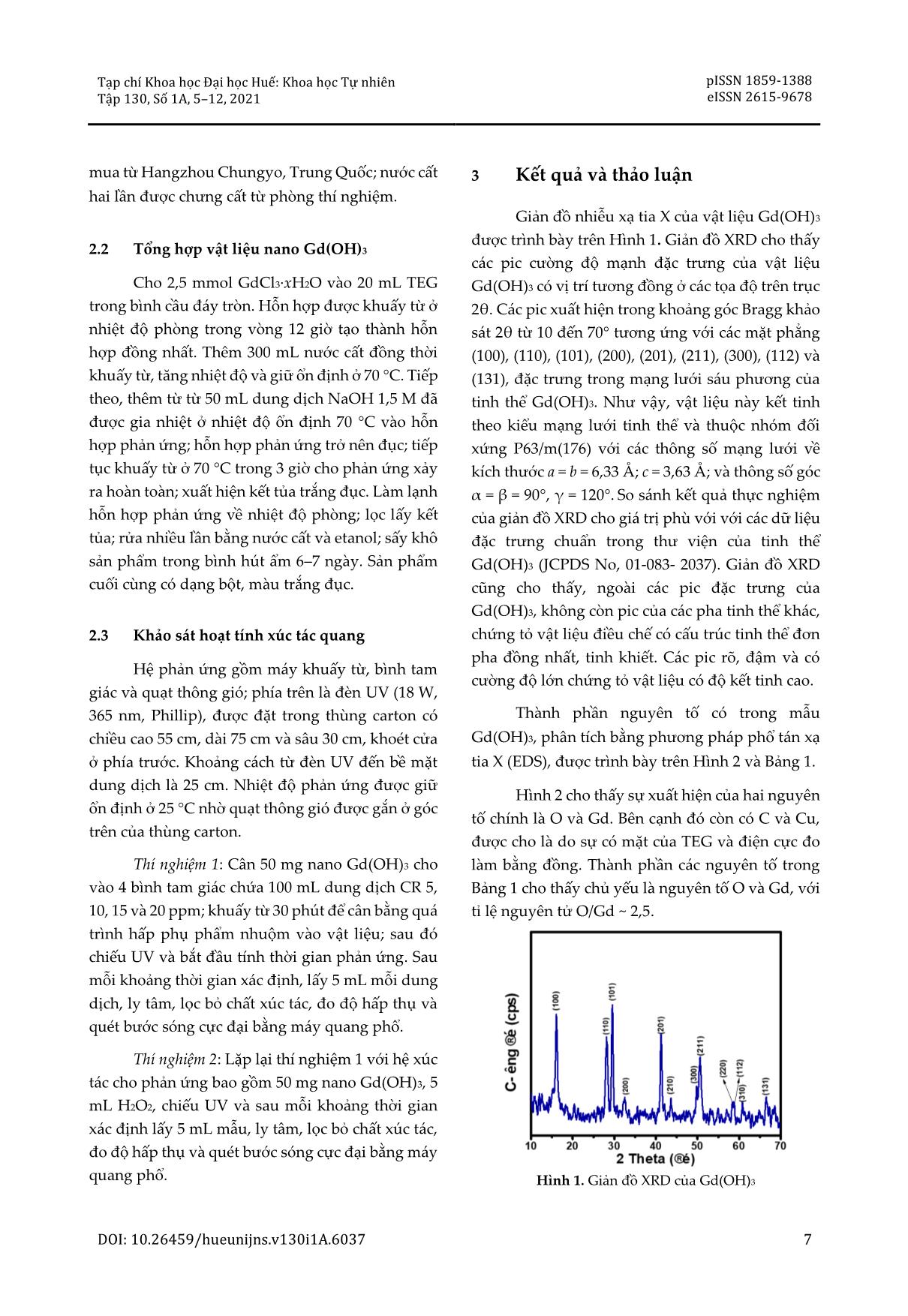
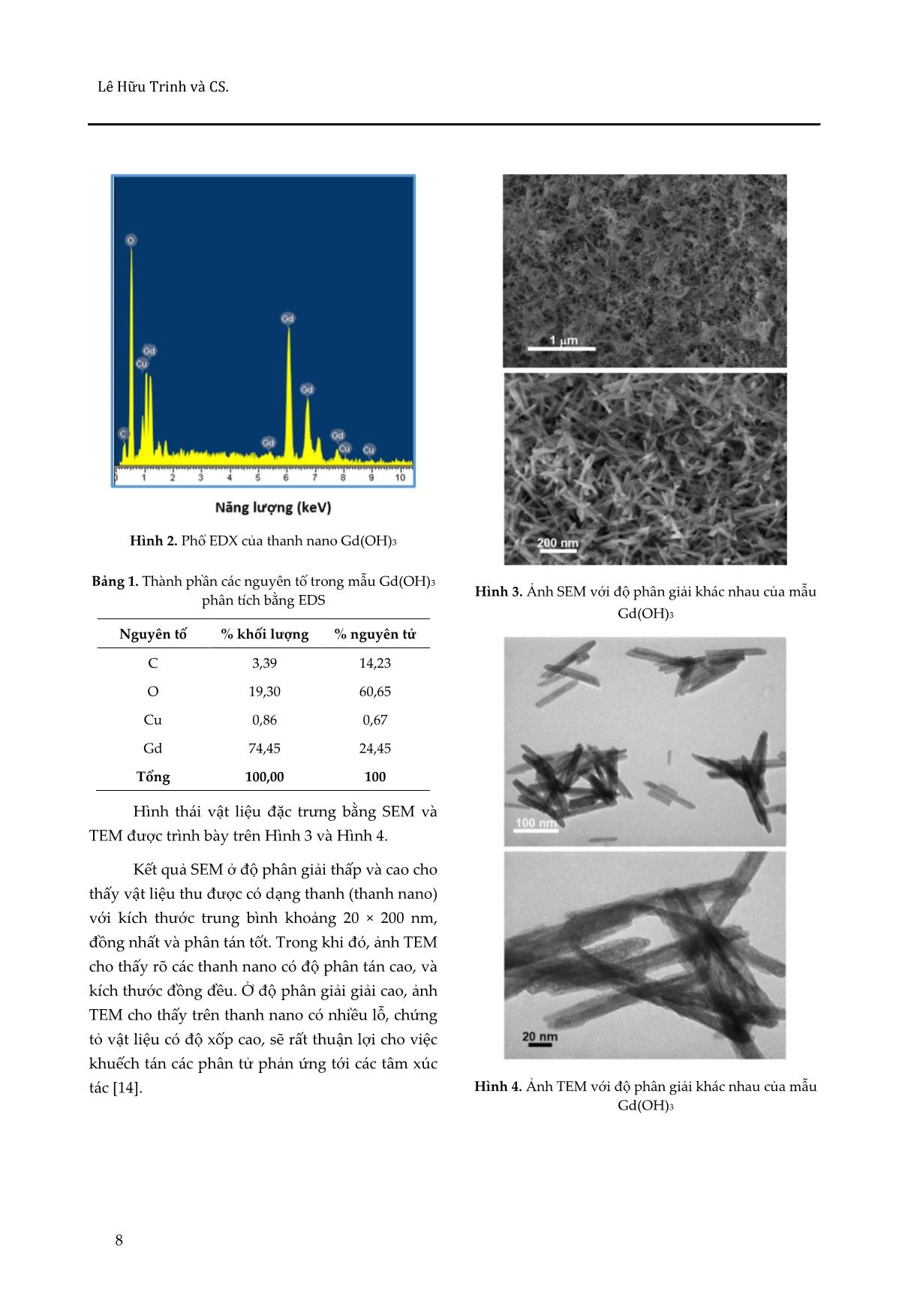
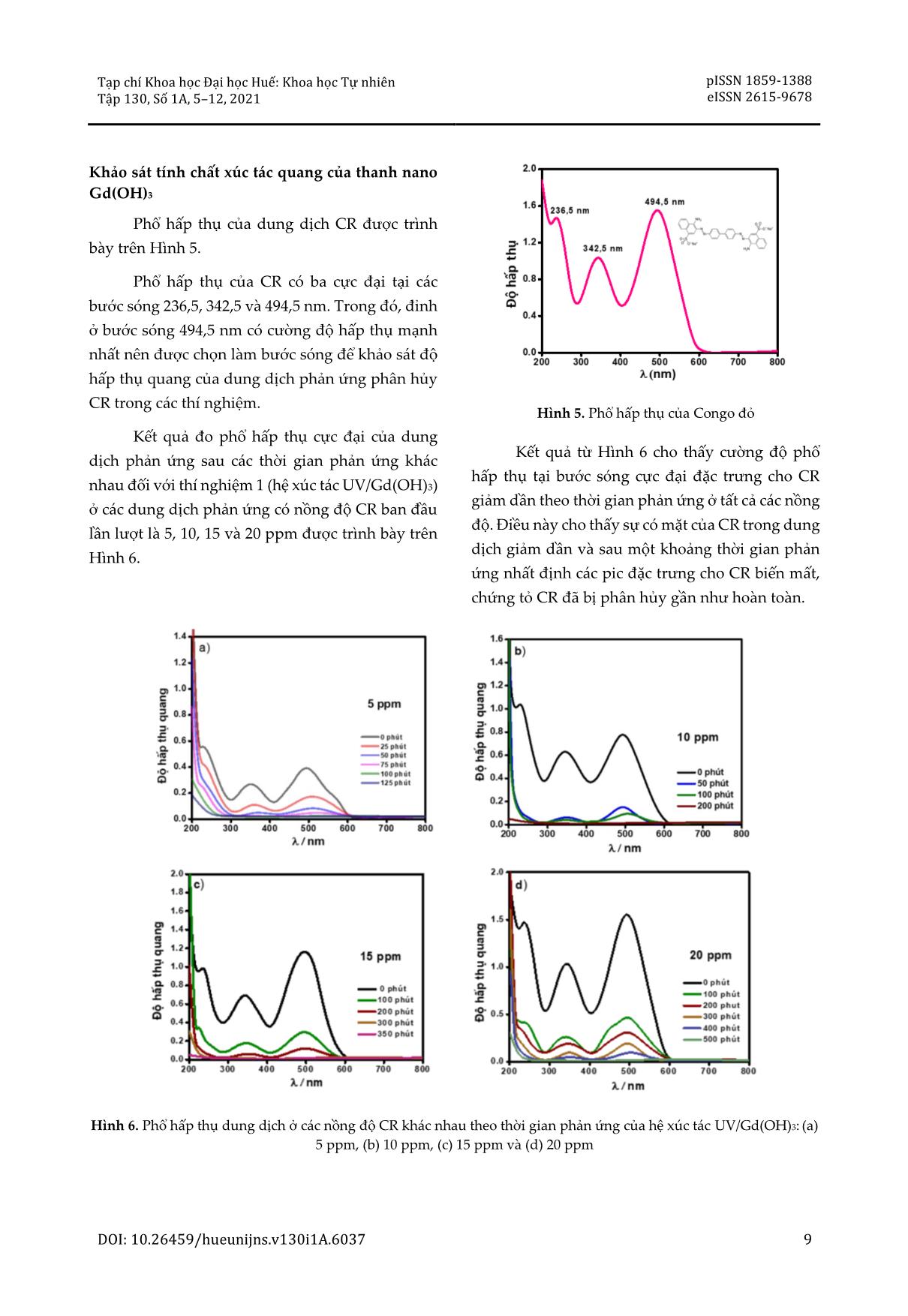
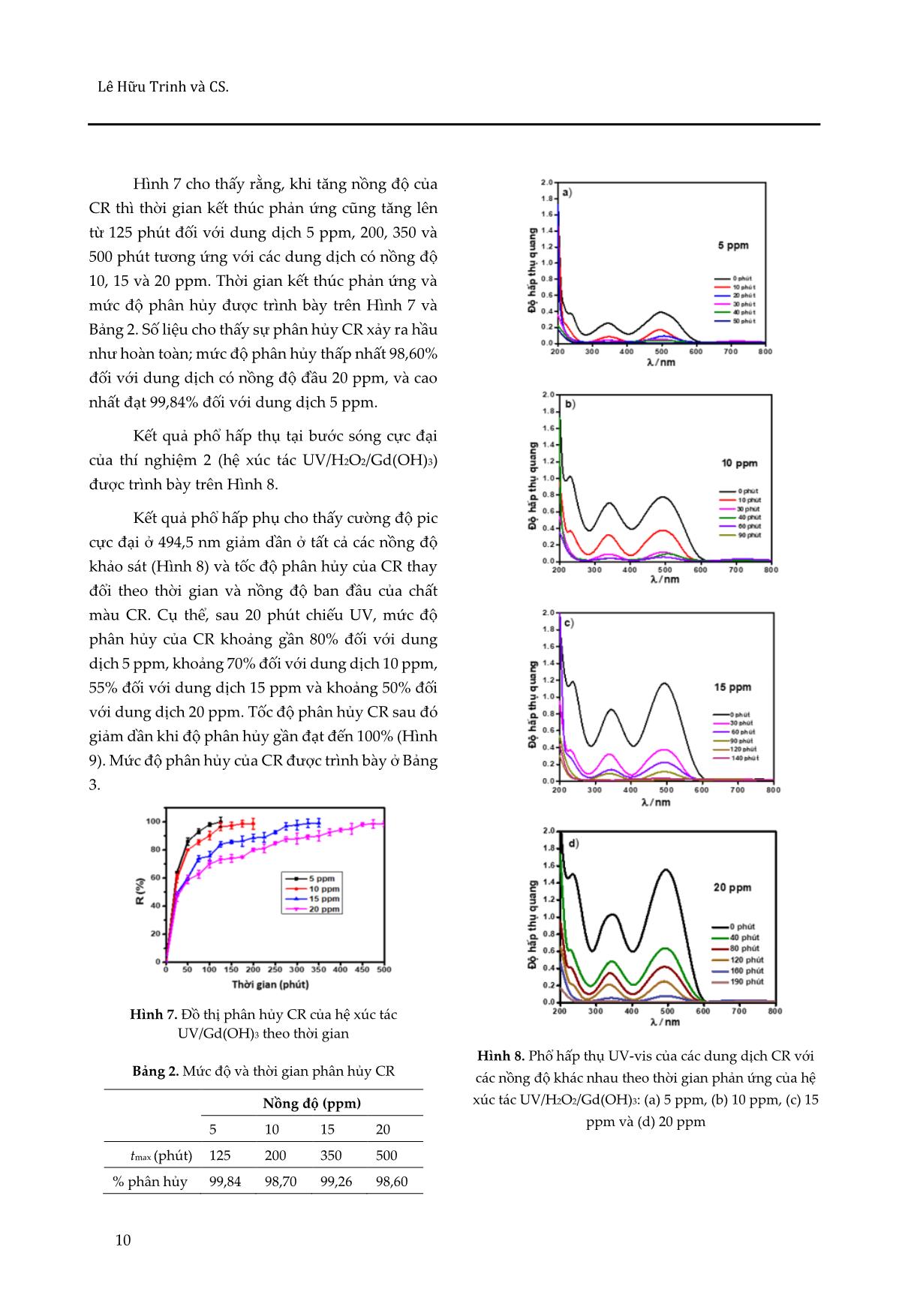
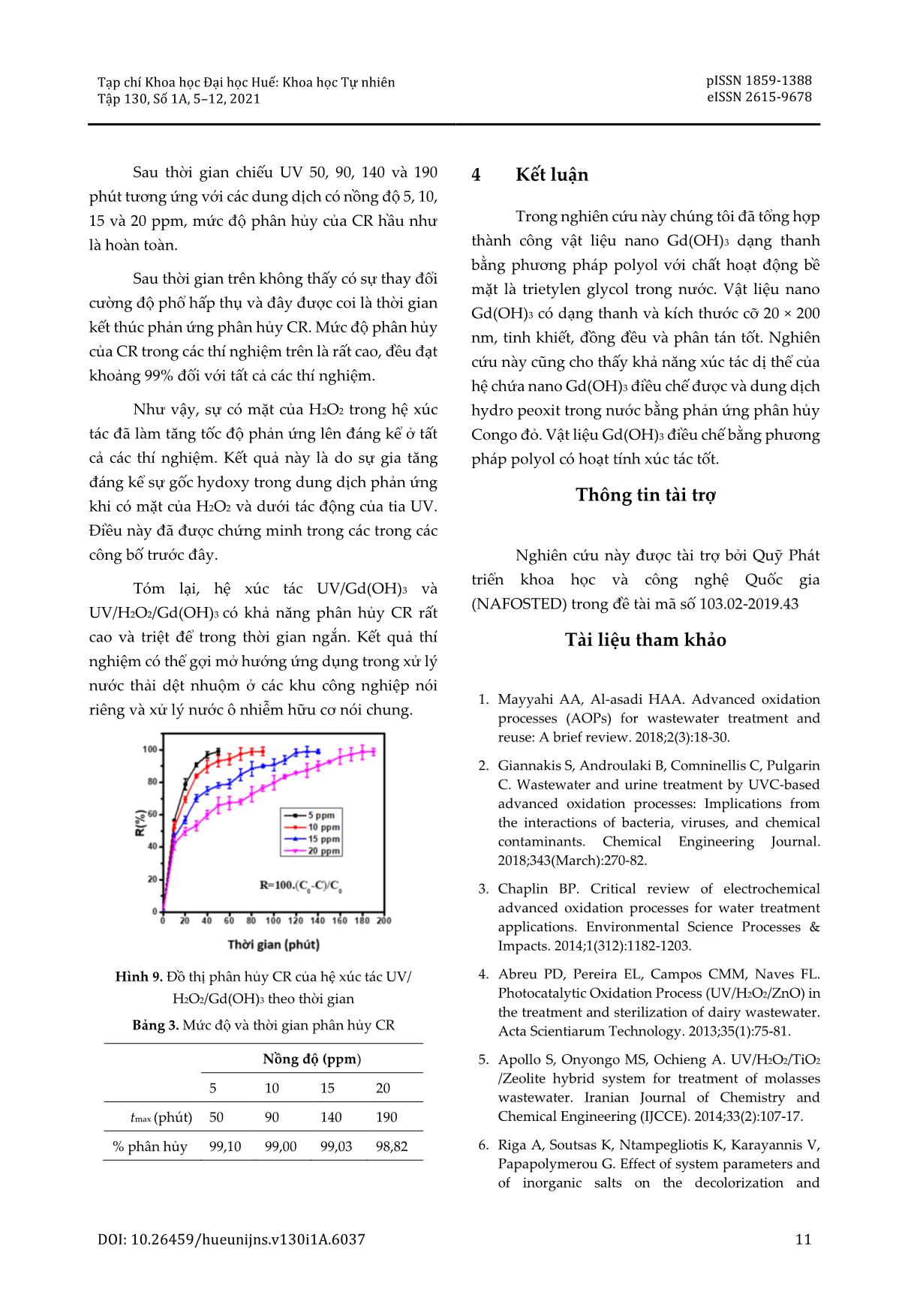
Tạp chí Khoa học Đại học Huế: Khoa học Tự nhiên pISSN 1859-1388 Tập 130, Số 1A, 5–12, 2021 eISSN 2615-9678 ĐIỀU CHẾ THANH NANO GADOLINI HYDROXIT VÀ KHẢO SÁT HOẠT TÍNH XÚC TÁC CỦA HỆ UV/H2O2/Gd(OH)3 Lê Hữu Trinh1,2*, Trần Thái Hòa1, Nguyễn Đức Cường3 1 Khoa Hóa học, Trường Đại học Khoa học, Đại học Huế, 77 Nguyễn Huệ, Huế, Việt Nam 2 Trường Cao đẳng Sư phạm Bà Rịa – Vũng Tàu, 689 Cách Mạng Tháng Tám, Tp. Bà Rịa, Việt Nam 3 Trường Du lịch, Đại học Huế, 22 Lâm Hoằng, Huế, Việt Nam * Tác giả liên hệ Lê Hữu Trinh (Ngày nhận bài: 02-10-2020; Ngày chấp nhận đăng: 18-12-2020) Tóm tắt. Trong nghiên cứu này, vật liệu nano Gd(OH)3 dạng thanh đã được tổng hợp bằng phương pháp polyol với tiền chất là gadolini clorua hydrat (GdCl3·xH2O), natri hydroxit và chất hoạt động bề mặt là trietylen glycol (C6H14O4). Sản phẩm đã được đặc trưng bằng các kỹ thuật XRD, SEM, TEM, TG- DTA, EDX. Kết quả cho thấy vật liệu Gd(OH)3 thu được có cấu trúc dạng thanh nano, đồng đều với khích thước 20 × 200 nm và tinh khiết. Vật liệu được ứng dụng trong phản ứng oxy hóa nâng cao đối với quang hóa phân hủy Congo đỏ của hệ xúc tác UV/Gd(OH)3 và UV/H2O2/Gd(OH)3. Từ khóa: Gd(OH)3, thanh nano, oxy hóa nâng cao, Congo đỏ Synthesis and catalytic performance of gadolinium hydroxide nanorods in Congo red decomposition with UV/H2O2/Gd(OH)3 system Le Huu Trinh1,2*, Tran Thai Hoa1, Nguyen Duc Cuong3 1 University of Sciences, Hue University, 77 Nguyen Hue St., Hue, Vietnam 2 Ba Ria – Vung Tau College of Education, 689 Cach Mang Thang Tam St., Ba Ria City, Vietnam 3 School of Hospitality and Tourism, Hue University, 22 Lam Hoang St., Hue, Vietnam * Correspondence to Le Huu Trinh (Received: 02 October 2020; Accepted: 18 December 2020) Abstract. In this study, nano Gd(OH)3 was synthesized with the polyol method with gadolinium chloride hydrate (GdCl3·xH2O) and sodium hydroxide as precursors, and triethylene glycol (C6H14O4) as a surfactant. The material was characterized with XRD, SEM, TEM, TG-DTA, EDX techniques. Gd(OH)3 has the form of pure nanorods with a uniform size of 20 × 200 nm. The material was utilized as a catalyst in the advanced photochemical decomposition of Congo red as the UV/Gd(OH)3 and UV/H2O2/Gd(OH)3 system. Keywords: Gd(OH)3, nanorod, advanced photochemical decomposition, Congo red DOI: 10.26459/hueunijns.v130i1A.6037 5 Lê Hữu Trinh và CS. 1 Mở đầu như ít thay đổi sau nhiều lần tái sử dụng và hàm lượng của CR đỏ bị phân hủy đạt trên 85% sau 200 Trong những năm gần đây, quá trình oxy phút phản ứng. hóa khử nâng cao đã được chứng minh là một Đối tượng nghiên cứu hoạt tính xúc tác trong những phương pháp hiệu quả, kinh tế cao và quang phân hủy thông thường là các hợp chất chứa có khả năng xử lý nguồn nước ô nhiễm hợp chất vòng thơm hoặc dị vòng, hợp chất màu azo hoặc hữu cơ tốt [1, 2]. Bản chất của quá trình oxy hóa các hợp chất hữu cơ gây ô nhiễm nguồn nước [10- khử nâng cao là tạo ra gốc tự do .OH, một sản phẩm 12]. Đây là những chất hữu cơ gây ô nhiễm, khó trung gian, có hoạt tính oxy hóa rất cao (E0 = 2,8 V), phân hủy và có độc tính cao xuất hiện ngày càng chỉ sau flo (E0 = 3,05 V) [1]. Gốc tự do hydoxy được nhiều trong quá trình sản xuất công nghiệp cũng tạo ra bởi các tác nhân H2O2, O3, H2O, v.v. dưới tác như các hoạt động kinh tế – xã hội; chúng đã và dụng của tia UV hoặc UV/xúc tác rắn [1-3]. Vật liệu đang gây ra những hệ lụy nặng nề về môi trường. xúc tác rắn thông thường được sử dụng là các hợp Trong đó, hợp chất màu azo được sử dụng làm chất của kim loại chuyển tiếp như oxit, hydroxit, thuốc nhuộm trong công nghiệp dệt may – sự phát sunfua, v.v. Trong đó, quá trình phản ứng oxy hóa triển của ngành dệt may kéo theo quá trình xả thải khử nâng cao trên chất xúc tác dị thể vẫn chưa các chất nhuộm gây ô nhiễm môi trường. Vì vậy, được nghiên cứu đầy đủ. Số lượng công trình được việc xử lý các hợp chất hữu cơ nói chung và chất công bố về hệ xúc tác UV/H2O2/xúc tác rắn vẫn còn màu azo trong nước thải được quan tâm nhiều, rất khiêm tốn, tiêu biểu là hệ UV/H2O2/ZnO xúc trong đó CR được nhiều tác giả chọn làm đối tượng tác quá trình xử lý nước thải của ngành công nghiên cứu trong các nghiên cứu sự phân hủy của nghiệp sữa [4], hoặc UV/H2O2/TiO2 và chất màu azo [9, 13]. UV/H2O2/TiO2+Zeolit được các tác giả nghiên cứu xúc tác cho quá trình phân hủy các chất màu trong Trong nghiên cứu này, vật liệu nano nước thải rỉ đường và nước thải chứa chất màu azo Gd(OH)3 dạng thanh được tổng hợp bằng phương trong sản phẩm thương mại [5, 6]. pháp polyol. Các đặc trưng cấu trúc và hình thái của sản phẩm Gd(OH)3 được nghiên cứu bằng các Vật liệu nano đất hiếm sử dụng trong xúc tác kỹ thuật hiện đại như XRD, SEM, TEM và EDX. oxy khử nâng cao còn rất ít được nghiên cứu, đặc Đồng thời, hoạt tính xúc tác quang oxy hóa khử biệt là vật liệu nano chứa oxy của gadolini. Các nâng cao dị thể của hệ UV/Gd(OH)3 và công trình nghiên cứu về nano của gadolini hầu hết UV/H2O2/Gd(OH)3 cũng được nghiên cứu trong đều cho thấy khả năng ứng dụng trong lĩnh vực phản ứng phân hủy CR. tương phản quang của kỹ thuật chụp cộng hưởng từ (MRI) [7, 8]. Nghiên cứu của Liu và cs. [9] là công trình hiếm hoi được công bố về tính chất xúc 2 Phương pháp tác của vật liệu nano chứa oxy của gadolini. Trong 2.1 Hóa chất và thiết bị công trình này, các nhà nghiên cứu đã điều chế thành công Gd(OH)3 dạng thanh nano với đường Tất cả hóa chất được sử dụng trong nghiên kính 10–30 nm và chiều dài lớn hơn 450 nm, hấp cứu này đều có độ tinh khiết cao: gadolini clorua thụ ánh sáng ở vùng tử ngoại gần (300–400 nm). hydrat (GdCl3·xH2O, 99,9%) được mua từ hãng Nhóm tác giả nghiên cứu tính chất xúc tác quang Sigma; natri hydroxit (NaOH, 99,99%), trietylen của vật liệu này khi mới điều chế và sau khi tái sử glycol (TEG) (HO(CH2)2O(CH2)2O(CH2)2OH, 99%), dụng trong hệ chứa Congo đỏ (CR) dưới tác dụng hydro peoxit (H2O2, 30%) mua từ hãng Merck, CR của tia UV. Kết quả cho thấy hoạt tính xúc tác hầu 6 Tạp chí Khoa học Đại học Huế: Khoa học Tự nhiên pISSN 1859-1388 Tập 130, Số 1A, 5–12, 2021 eISSN 2615-9678 mua từ Hangzhou Chungyo, Trung Quốc; nước cất 3 Kết quả và thảo luận hai lần được chưng cất từ phòng thí nghiệm. Giản đồ nhiễu xạ tia X của vật liệu Gd(OH)3 được trình bày trên Hình 1. Giản đồ XRD cho thấy 2.2 Tổng hợp vật liệu nano Gd(OH)3 các pic cường độ mạnh đặc trưng của vật liệu Cho 2,5 mmol GdCl3·xH2O vào 20 mL TEG Gd(OH)3 có vị trí tương đồng ở các tọa độ trên trục trong bình cầu đáy tròn. Hỗn hợp được khuấy từ ở 2θ. Các pic xuất hiện trong khoảng góc Bragg khảo nhiệt độ phòng trong vòng 12 giờ tạo thành hỗn sát 2θ từ 10 đến 70° tương ứng với các mặt phẳng hợp đồng nhất. Thêm 300 mL nước cất đồng thời (100), (110), (101), (200), (201), (211), (300), (112) và khuấy từ, tăng nhiệt độ và giữ ổn định ở 70 °C. Tiếp (131), đặc trưng trong mạng lưới sáu phương của theo, thêm từ từ 50 mL dung dịch NaOH 1,5 M đã tinh thể Gd(OH)3. Như vậy, vật liệu này kết tinh được gia nhiệt ở nhiệt độ ổn định 70 °C vào hỗn theo kiểu mạng lưới tinh thể và thuộc nhóm đối hợp phản ứng; hỗn hợp phản ứng trở nên đục; tiếp xứng P63/m(176) với các thông số mạng lưới về tục khuấy từ ở 70 °C trong 3 giờ cho phản ứng xảy kích thước a = b = 6,33 Å; c = 3,63 Å; và thông số góc ra hoàn toàn; xuất hiện kết tủa trắng đục. Làm lạnh α = β = 90°, γ = 120°. So sánh kết quả thực nghiệm hỗn hợp phản ứng về nhiệt độ phòng; lọc lấy kết của giản đồ XRD cho giá trị phù với với các dữ liệu tủa; rửa nhiều lần bằng nước cất và etanol; sấy khô đặc trưng chuẩn trong thư viện của tinh thể sản phẩm trong bình hút ẩm 6–7 ngày. Sản phẩm Gd(OH)3 (JCPDS No, 01-083- 2037). Giản đồ XRD cuối cùng có dạng bột, màu trắng đục. cũng cho thấy, ngoài các pic đặc trưng của Gd(OH)3, không còn pic của các pha tinh thể khác, 2.3 Khảo sát hoạt tính xúc tác quang chứng tỏ vật liệu điều chế có cấu trúc tinh thể đơn pha đồng nhất, tinh khiết. Các pic rõ, đậm và có Hệ phản ứng gồm máy khuấy từ, bình tam cường độ lớn chứng tỏ vật liệu có độ kết tinh cao. giác và quạt thông gió; phía trên là đèn UV (18 W, 365 nm, Phillip), được đặt trong thùng carton có Thành phần nguyên tố có trong mẫu chiều cao 55 cm, dài 75 cm và sâu 30 cm, khoét cửa Gd(OH)3, phân tích bằng phương pháp phổ tán xạ ở phía trước. Khoảng cách từ đèn UV đến bề mặt tia X (EDS), được trình bày trên Hình 2 và Bảng 1. dung dịch là 25 cm. Nhiệt độ phản ứng được giữ Hình 2 cho thấy sự xuất hiện của hai nguyên ổn định ở 25 °C nhờ quạt thông gió được gắn ở góc tố chính là O và Gd. Bên cạnh đó còn có C và Cu, trên của thùng carton. được cho là do sự có mặt của TEG và điện cực đo Thí nghiệm 1: Cân 50 mg nano Gd(OH)3 cho làm bằng đồng. Thành phần các nguyên tố trong vào 4 bình tam giác chứa 100 mL dung dịch CR 5, Bảng 1 cho thấy chủ yếu là nguyên tố O và Gd, với 10, 15 và 20 ppm; khuấy từ 30 phút để cân bằng quá tỉ lệ nguyên tử O/Gd ~ 2,5. trình hấp phụ phẩm nhuộm vào vật liệu; sau đó chiếu UV và bắt đầu tính thời gian phản ứng. Sau mỗi khoảng thời gian xác định, lấy 5 mL mỗi dung dịch, ly tâm, lọc bỏ chất xúc tác, đo độ hấp thụ và quét bước sóng cực đại bằng máy quang phổ. Thí nghiệm 2: Lặp lại thí nghiệm 1 với hệ xúc tác cho phản ứng bao gồm 50 mg nano Gd(OH)3, 5 mL H2O2, chiếu UV và sau mỗi khoảng thời gian xác định lấy 5 mL mẫu, ly tâm, lọc bỏ chất xúc tác, đo độ hấp thụ và quét bước sóng cực đại bằng máy quang phổ. Hình 1. Giản đồ XRD của Gd(OH)3 DOI: 10.26459/hueunijns.v130i1A.6037 7 Lê Hữu Trinh và CS. Hình 2. Phổ EDX của thanh nano Gd(OH)3 Bảng 1. Thành phần các nguyên tố trong mẫu Gd(OH)3 Hình 3. Ảnh SEM với độ phân giải khác nhau của mẫu phân tích bằng EDS Gd(OH)3 Nguyên tố % khối lượng % nguyên tử C 3,39 14,23 O 19,30 60,65 Cu 0,86 0,67 Gd 74,45 24,45 Tổng 100,00 100 Hình thái vật liệu đặc trưng bằng SEM và TEM được trình bày trên Hình 3 và Hình 4. Kết quả SEM ở độ phân giải thấp và cao cho thấy vật liệu thu được có dạng thanh (thanh nano) với kích thước trung bình khoảng 20 × 200 nm, đồng nhất và phân tán tốt. Trong khi đó, ảnh TEM cho thấy rõ các thanh nano có độ phân tán cao, và kích thước đồng đều. Ở độ phân giải giải cao, ảnh TEM cho thấy trên thanh nano có nhiều lỗ, chứng tỏ vật liệu có độ xốp cao, sẽ rất thuận lợi cho việc khuếch tán các phân tử phản ứng tới các tâm xúc tác [14]. Hình 4. Ảnh TEM với độ phân giải khác nhau của mẫu Gd(OH)3 8 Tạp chí Khoa học Đại học Huế: Khoa học Tự nhiên pISSN 1859-1388 Tập 130, Số 1A, 5–12, 2021 eISSN 2615-9678 Khảo sát tính chất xúc tác quang của thanh nano Gd(OH)3 Phổ hấp thụ của dung dịch CR được trình bày trên Hình 5. Phổ hấp thụ của CR có ba cực đại tại các bước sóng 236,5, 342,5 và 494,5 nm. Trong đó, đỉnh ở bước sóng 494,5 nm có cường độ hấp thụ mạnh nhất nên được chọn làm bước sóng để khảo sát độ hấp thụ quang của dung dịch phản ứng phân hủy CR trong các thí nghiệm. Hình 5. Phổ hấp thụ của Congo đỏ Kết quả đo phổ hấp thụ cực đại của dung Kết quả từ Hình 6 cho thấy cường độ phổ dịch phản ứng sau các thời gian phản ứng khác hấp thụ tại bước sóng cực đại đặc trưng cho CR nhau đối với thí nghiệm 1 (hệ xúc tác UV/Gd(OH)3) giảm dần theo thời gian phản ứng ở tất cả các nồng ở các dung dịch phản ứng có nồng độ CR ban đầu độ. Điều này cho thấy sự có mặt của CR trong dung lần lượt là 5, 10, 15 và 20 ppm được trình bày trên dịch giảm dần và sau một khoảng thời gian phản Hình 6. ứng nhất định các pic đặc trưng cho CR biến mất, chứng tỏ CR đã bị phân hủy gần như hoàn toàn. Hình 6. Phổ hấp thụ dung dịch ở các nồng độ CR khác nhau theo thời gian phản ứng của hệ xúc tác UV/Gd(OH)3: (a) 5 ppm, (b) 10 ppm, (c) 15 ppm và (d) 20 ppm DOI: 10.26459/hueunijns.v130i1A.6037 9 Lê Hữu Trinh và CS. Hình 7 cho thấy rằng, khi tăng nồng độ của CR thì thời gian kết thúc phản ứng cũng tăng lên từ 125 phút đối với dung dịch 5 ppm, 200, 350 và 500 phút tương ứng với các dung dịch có nồng độ 10, 15 và 20 ppm. Thời gian kết thúc phản ứng và mức độ phân hủy được trình bày trên Hình 7 và Bảng 2. Số liệu cho thấy sự phân hủy CR xảy ra hầu như hoàn toàn; mức độ phân hủy thấp nhất 98,60% đối với dung dịch có nồng độ đầu 20 ppm, và cao nhất đạt 99,84% đối với dung dịch 5 ppm. Kết quả phổ hấp thụ tại bước sóng cực đại của thí nghiệm 2 (hệ xúc tác UV/H2O2/Gd(OH)3) được trình bày trên Hình 8. Kết quả phổ hấp phụ cho thấy cường độ pic cực đại ở 494,5 nm giảm dần ở tất cả các nồng độ khảo sát (Hình 8) và tốc độ phân hủy của CR thay đổi theo thời gian và nồng độ ban đầu của chất màu CR. Cụ thể, sau 20 phút chiếu UV, mức độ phân hủy của CR khoảng gần 80% đối với dung dịch 5 ppm, khoảng 70% đối với dung dịch 10 ppm, 55% đối với dung dịch 15 ppm và khoảng 50% đối với dung dịch 20 ppm. Tốc độ phân hủy CR sau đó giảm dần khi độ phân hủy gần đạt đến 100% (Hình 9). Mức độ phân hủy của CR được trình bày ở Bảng 3. Hình 7. Đồ thị phân hủy CR của hệ xúc tác UV/Gd(OH)3 theo thời gian Hình 8. Phổ hấp thụ UV-vis của các dung dịch CR với Bảng 2. Mức độ và thời gian phân hủy CR các nồng độ khác nhau theo thời gian phản ứng của hệ Nồng độ (ppm) xúc tác UV/H2O2/Gd(OH)3: (a) 5 ppm, (b) 10 ppm, (c) 15 ppm và (d) 20 ppm 5 10 15 20 tmax (phút) 125 200 350 500 % phân hủy 99,84 98,70 99,26 98,60 10 Tạp chí Khoa học Đại học Huế: Khoa học Tự nhiên pISSN 1859-1388 Tập 130, Số 1A, 5–12, 2021 eISSN 2615-9678 Sau thời gian chiếu UV 50, 90, 140 và 190 4 Kết luận phút tương ứng với các dung dịch có nồng độ 5, 10, 15 và 20 ppm, mức độ phân hủy của CR hầu như Trong nghiên cứu này chúng tôi đã tổng hợp là hoàn toàn. thành công vật liệu nano Gd(OH)3 dạng thanh bằng phương pháp polyol với chất hoạt động bề Sau thời gian trên không thấy có sự thay đổi mặt là trietylen glycol trong nước. Vật liệu nano cường độ phổ hấp thụ và đây được coi là thời gian Gd(OH)3 có dạng thanh và kích thước cỡ 20 × 200 kết thúc phản ứng phân hủy CR. Mức độ phân hủy nm, tinh khiết, đồng đều và phân tán tốt. Nghiên của CR trong các thí nghiệm trên là rất cao, đều đạt cứu này cũng cho thấy khả năng xúc tác dị thể của khoảng 99% đối với tất cả các thí nghiệm. hệ chứa nano Gd(OH)3 điều chế được và dung dịch Như vậy, sự có mặt của H2O2 trong hệ xúc hydro peoxit trong nước bằng phản ứng phân hủy tác đã làm tăng tốc độ phản ứng lên đáng kể ở tất Congo đỏ. Vật liệu Gd(OH)3 điều chế bằng phương cả các thí nghiệm. Kết quả này là do sự gia tăng pháp polyol có hoạt tính xúc tác tốt. đáng kể sự gốc hydoxy trong dung dịch phản ứng Thông tin tài trợ khi có mặt của H2O2 và dưới tác động của tia UV. Điều này đã được chứng minh trong các trong các công bố trước đây. Nghiên cứu này được tài trợ bởi Quỹ Phát triển khoa học và công nghệ Quốc gia Tóm lại, hệ xúc tác UV/Gd(OH)3 và (NAFOSTED) trong đề tài mã số 103.02-2019.43 UV/H2O2/Gd(OH)3 có khả năng phân hủy CR rất cao và triệt để trong thời gian ngắn. Kết quả thí Tài liệu tham khảo nghiệm có thể gợi mở hướng ứng dụng trong xử lý nước thải dệt nhuộm ở các khu công nghiệp nói 1. Mayyahi AA, Al-asadi HAA. Advanced oxidation riêng và xử lý nước ô nhiễm hữu cơ nói chung. processes (AOPs) for wastewater treatment and reuse: A brief review. 2018;2(3):18-30. 2. Giannakis S, Androulaki B, Comninellis C, Pulgarin C. Wastewater and urine treatment by UVC-based advanced oxidation processes: Implications from the interactions of bacteria, viruses, and chemical contaminants. Chemical Engineering Journal. 2018;343(March):270-82. 3. Chaplin BP. Critical review of electrochemical advanced oxidation processes for water treatment applications. Environmental Science Processes & Impacts. 2014;1(312):1182-1203. Hình 9. Đồ thị phân hủy CR của hệ xúc tác UV/ 4. Abreu PD, Pereira EL, Campos CMM, Naves FL. Photocatalytic Oxidation Process (UV/H2O2/ZnO) in H2O2/Gd(OH)3 theo thời gian the treatment and sterilization of dairy wastewater. Bảng 3. Mức độ và thời gian phân hủy CR Acta Scientiarum Technology. 2013;35(1):75-81. Nồng độ (ppm) 5. Apollo S, Onyongo MS, Ochieng A. UV/H2O2/TiO2 /Zeolite hybrid system for treatment of molasses 5 10 15 20 wastewater. Iranian Journal of Chemistry and tmax (phút) 50 90 140 190 Chemical Engineering (IJCCE). 2014;33(2):107-17. % phân hủy 99,10 99,00 99,03 98,82 6. Riga A, Soutsas K, Ntampegliotis K, Karayannis V, Papapolymerou G. Effect of system parameters and of inorganic salts on the decolorization and DOI: 10.26459/hueunijns.v130i1A.6037 11 Lê Hữu Trinh và CS. degradation of Procion H-exl dyes. Comparison of magnetite + H2O2 + UV process. International H2O2/UV, Fenton, UV/Fenton, TiO2/UV and Journal of Environmental Science and Development. TiO2/UV/H2O2. Desalination. 2007;211(1-3):72-86. 2016;7(5):325-329. 7. Rogosnitzky M, Branch S. Gadolinium-based 12. Gnanaprakasam A, Sivakumar VM, Thirumarimurugan contrast agent toxicity: a review of known and M. Influencing parameters in the photocatalytic proposed mechanisms. BioMetals. 2016;29(3):365- degradation of organic effluent via nanometal oxide 376. catalyst: a review. Indian Journal of Materials Science. 2015;2015:1-16. 8. Jiang X, Yu L, Yao C, Zhang F, Zhang J, Li C. Synthesis and characterization of Gd2O3 hollow 13. Vidya YS, Anantharaju KS, Nagabhushana H, microspheres using a template-directed method. Sharma SC. Euphorbia tirucalli mediated green Materials. 2016;9(5):323. synthesis of rose like morphology of Gd2O3:Eu3+ red phosphor: Structural, photoluminescence and 9. Liu S, Cai Y, Cai X, Li H, Zhang F, Mu Q, et al. photocatalytic studies. Journal of Alloys and Catalytic photodegradation of Congo red in Compounds. 2015;619:760-70. aqueous solution by Ln(OH)3 (Ln = Nd, Sm, Eu, Gd, Tb, and Dy) nanorods. Applied Catalysis A: 14. Cuong ND, Hoa ND, Hoa TT, Khieu DQ, Quang DT, General. 2013;453:45-53. Quang VV, et al. Nanoporous hematite nanoparticles: Synthesis and applications for 10. Nan M, Sharma AK, Burn S, Saint CP. Feasibility benzylation of benzene and aromatic compounds. study on the application of advanced oxidation Journal of Alloys and Compounds. 2014;582:83-7. technologies for decentralised wastewater treatment. Journal of Cleaner Production. 2012;35:230-238. 11. Reza KM, Kurny A, Gulshan F, Dye AMB. Photocatalytic degradation of methylene blue by 12
File đính kèm:
 dieu_che_thanh_nano_gadolini_hydroxit_va_khao_sat_hoat_tinh.pdf
dieu_che_thanh_nano_gadolini_hydroxit_va_khao_sat_hoat_tinh.pdf

