Bài giảng Hóa học Lớp 9 - Tiết 37: Axit cacbonic và muối cacbonat
I. AXIT CACBONIC (H2CO3)
1. Trạng thái tự nhiên và tính chất vật lí
- CO2 tan được trong nước tạo thành dung dịch H2CO3
- Tỷ lệ VCO2 : VH2O = 9:100
2. Tính chất hoá học
- H2CO3 là axit yếu, dung dịch H2CO3 làm quỳ tím chuyển sang màu đỏ nhạt.
- H2CO3 là một axit không bền trong phản ứng bị phân huỷ:

Trang 1
Trang 2
Trang 3

Trang 4

Trang 5

Trang 6
Trang 7
Trang 8
Trang 9

Trang 10
Tải về để xem bản đầy đủ
Bạn đang xem 10 trang mẫu của tài liệu "Bài giảng Hóa học Lớp 9 - Tiết 37: Axit cacbonic và muối cacbonat", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Bài giảng Hóa học Lớp 9 - Tiết 37: Axit cacbonic và muối cacbonat

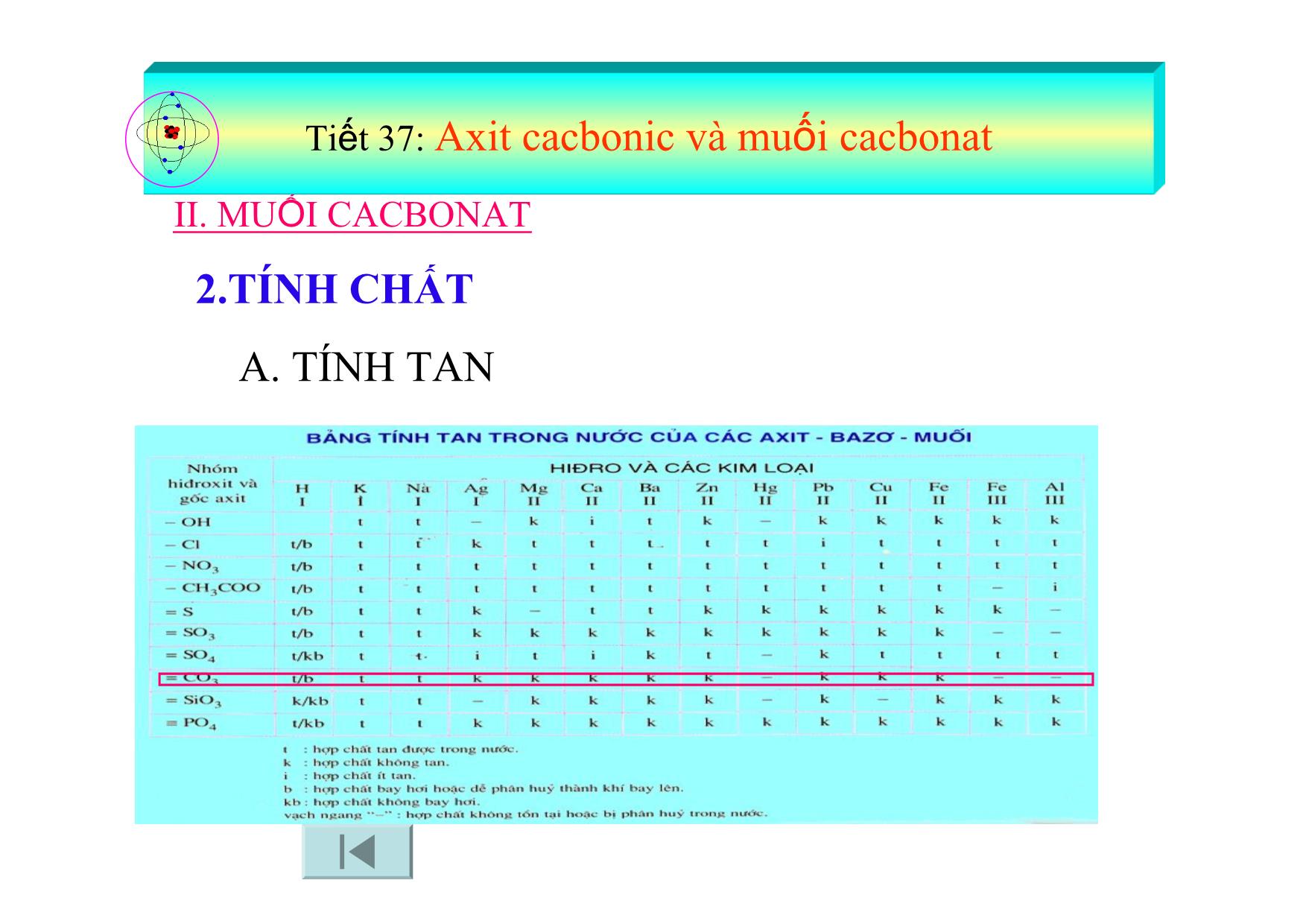
HÓA HỌC 9 AXIT CACBONIC VÀ MUỐI CACBONAT Em hãy chọn những chất thích hợp để điền vào các phương trình hoá học sau: 0t + Muối Muối mới Axit mớia b c d Muối Muối Muối Muối mới Muối mới + Bazơ mới Muối mới + + + + + CÂU HỎI: 0t Nhiều chất mới Axit Bazơ Muối ĐÁP ÁN 0t Muối Muối mới Axit mớia b c d Muối Muối Muối Muối mới Muối mới + Bazơ mới Muối mới+ + + + + Tiết 37: Axit cacbonic và muối cacbonat I. AXIT CACBONIC II. MUỐI CACBONAT III. CHU TRÌNH CACBON TRONG TỰ NHIÊN I. AXIT CACBONIC (H2CO3) 1. Trạng thái tự nhiên và tính chất vật lí - CO2 tan được trong nước tạo thành dung dịch H2CO3 - Tỷ lệ VCO2 : VH2O = 9:100 2. Tính chất hoá học - H2CO3 là axit yếu, dung dịch H2CO3 làm quỳ tím chuyển sang màu đỏ nhạt. - H2CO3 là một axit không bền trong phản ứng bị phân huỷ: H2CO3 CO2 + H2O Tiết 37: Axit cacbonic và muối cacbonat II. MUỐI CACBONAT 1. PHÂN LOẠI - Thế nào là muối cacbonat? - Dựa vào sự có hoặc không có nguyên tử H trong gốc axit ta có thể chia muối cacbonat thành mấy loại? Cho ví dụ? - Muối cacbonat là muối của axit cacbonic. -Có hai loại muối cacbonat: + Muối cacbonat trung hoà được gọi là muối cacbonat: + Muối cacbonat axit được gọi là muối hiđrocacbonat: ...,, 32323 COKCONaCaCO ...3,, 233 HCOCaKHCONaHCO Tiết 37: Axit cacbonic và muối cacbonat II. MUỐI CACBONAT 2.TÍNH CHẤT A. TÍNH TAN Tiết 37: Axit cacbonic và muối cacbonat - Đa số muối cacbonat không tan trong nước, trừ một số muối cacbonat của kim loại kiềm như: - Hầu hết muối hidrocacbonat tan trong nước như: ..., 3232 COKCONa ...3,3 22 HCOCaHCOMg II. MUỐI CACBONAT 2.TÍNH CHẤT A. TÍNH TAN Tiết 37: Axit cacbonic và muối cacbonat II. MUỐI CACBONAT 2. TÍNH CHẤT a. TÍNH TAN b. TÍNH CHẤT HOÁ HỌC - Dựa vào những tính chất hoá học của muối, em hãy dự đoán tính chất hoá học của muối cacbonat? Tác dụng với axit. * Thí nghiệm 1: dd và lần lượt td với HCl - Chuẩn bị: Hai ống nghiệm, mỗi ống nghiệm chứa khoảng 1ml dd và riêng biệt. Lọ đựng dd HCl, kẹp gỗ, ống hút, giá thí nghiệm. NaHCO3 CONa 32NaHCO3 CONa 32 Tiết 37: Axit cacbonic và muối cacbonat Tiến hành thí nghiệm Nhỏ vài giọt dd HCl vào hai ống nghiệm có chứa 1 ml Na2CO3 và 1 ml NaHCO3. Quan sát hiện tượng và giải thích? Hiện Tượng thí nghiệm Có bọt khí thoát ra ở cả hai ống nghiệm. Nhận xét, viết phương trinh phản ứng lkdddddd lkdddddd OHCONaClHClCONa OHCONaClHClNaHCO 2232 223 22 Đó là do có phản ứng hoá học sau: Tiết 37: Axit cacbonic và muối cacbonat * MUỐI CACBONAT + AXIT MẠNH MUỐI MỚI + CO2 + H2O Tác dụng với dd bazơ (Kiềm). * Thí nghiệm 2: dd tác dụng với dd - Chuẩn bị: Một ống nghiệm chứa khoảng 1ml dd và lọ đựng dd - Kẹp gỗ, giá thí nghiệm. Cách tiến hành: Nhỏ vài giọt dd vào ống nghiệm có chứa 1 ml Quan sát hiện tượng và giải thích: 32COK 2)(OHCa 32COK II. MUỐI CACBONAT 2.TÍNH CHẤT 2)(OHCa32COK 2)(OHCa Tiết 37: Axit cacbonic và muối cacbonat •Chú ý: •Muối hiđrocacbonat + dd kiềm muối trung hoà + H2O )()()()(: 2323 lOHddCONaddNaOHddNaHCOVD Nhận xét: Đó là do có phản ứng hoá học sau: )(2)()()( 3232 ddKOHrCaCOOHCaddCOK (Trắng) * MỘT SỐ DD MUỐI CACBONAT + DD BAZƠ MUỐI CABONAT KHÔNG TAN + BAZƠ MỚI Hiện tượng: Có vẩn đục hoặc kết tủa trắng xuất hiện. Tiết 37: Axit cacbonic và muối cacbonat Tác dụng với dd muối. * Thí nghiệm 3: dd tác dụng với dd - Chuẩn bị: Một ống nghiệm chứa khoảng 1ml dd và lọ đựng dd - Kẹp gỗ, ống hút, giá thí nghiệm. Cách tiến hành: Nhỏ vài giọt dd vào ống nghiệm có chứa 1 ml Quan sát hiện tượng và giải thích? 32CONa 2CaCl 2CaCl 32CONa 32CONa 2CaCl Tiết 37: Axit cacbonic và muối cacbonat Hiện tượng: Có vẩn đục hoặc kết tủa trắng xuất hiện. Nhận xét: Đó là do có phản ứng hoá học sau: )(2)()()( 3232 ddNaClrCaCOddCaClddCONa (Trắng) * DD MUỐI CACBONAT + MỘT SỐ DD MUỐI KHÁC 2 MUỐI MỚI. II. MUỐI CACBONAT 2.TÍNH CHẤT Tiết 37: Axit cacbonic và muối cacbonat Muối cacbonat bị nhiệt phân huỷ Quan sát Hình 3.16 hãy hoàn thành sơ đồ phản ứng sau: to Na2CO3++ Đáp án: NaHCO3 to Na2CO3+CO2+H2O Muối cacbonat bị nhiệt phân huỷ 3. Ứng dụng (SGK) III. CHU TRÌNH CACBON TRONG TỰ NHIÊN Bài tập: Hãy cho biết các cặp chất sau đây, cặp nào có thể tác dụng với nhau: a. và b. và NaCl c. và HCl d. và e. và Giải thích và viết phương trình hoá học? 42SOH 3KHCO 32COK 3MgCO 2)(OHBa 2CaCl 32COK 32CONa OHCOSOKKHCOSOHa 2242342 222. NaClCOK 32b. Không phản ứng NaClCaCOCONaCaCl 23322 c. d. OHCOMgClHClMgCO 2223 2 KOHBaCOCOKOHBa 2)( 3322 e. Đáp án: Bài tập về nhà: 1, 2, 3, 5 SGK (Trang 91) + Bài tập bổ sung SBT Chuẩn bị bài 30: Silic. Công nghiệp silicat KÍNH CHÚC CÁC THẦY CÔ GIÁO MẠNH KHOẺ - HẠNH PHÚC. CHÚC CÁC EM HỌC SINH CHĂM NGOAN - HỌC GIỎI! Quan sát Hình 3.16 hãy hoàn thành sơ đồ phản ứng sau: OHCOCONaNaHCO t 22323 02
File đính kèm:
 bai_giang_hoa_hoc_lop_9_tiet_37_axit_cacbonic_va_muoi_cacbon.pdf
bai_giang_hoa_hoc_lop_9_tiet_37_axit_cacbonic_va_muoi_cacbon.pdf

